세계 최초의 중증 퇴행성관절염 치료제 “조인트스템” 국내 임상 3상 탑라인 결과 발표
-1차 평가지표 WOMAC(관절 기능)과 VAC(통증) 모두 통계적 유의성 확보
-통계 유의성 성패 가늠하는 ‘P’값 기준 0.05보다 월등히 좋은 결과 도출
네이처셀이 관계사인 알바이오가 개발하고 있는 세계 최초의 자가지방 유래 중간엽줄기세포를 이용한 중증 무릎 퇴행성관절염 치료제 ‘조인트스템’의 국내 3상 임상시험 유효성 평가 탑라인(Topline) 결과를 15일 발표했다.
임상시험 수탁기관(CRO)인 LSK Global PS가 유효성 평가 데이터를 분석한 결과, 1차 평가지표인 WOMAC(골관절염 지수)과 VAS(통증 지수) 모두 위약 대비 통계적으로 유의하게 개선되어 우월성이 확인됐다.
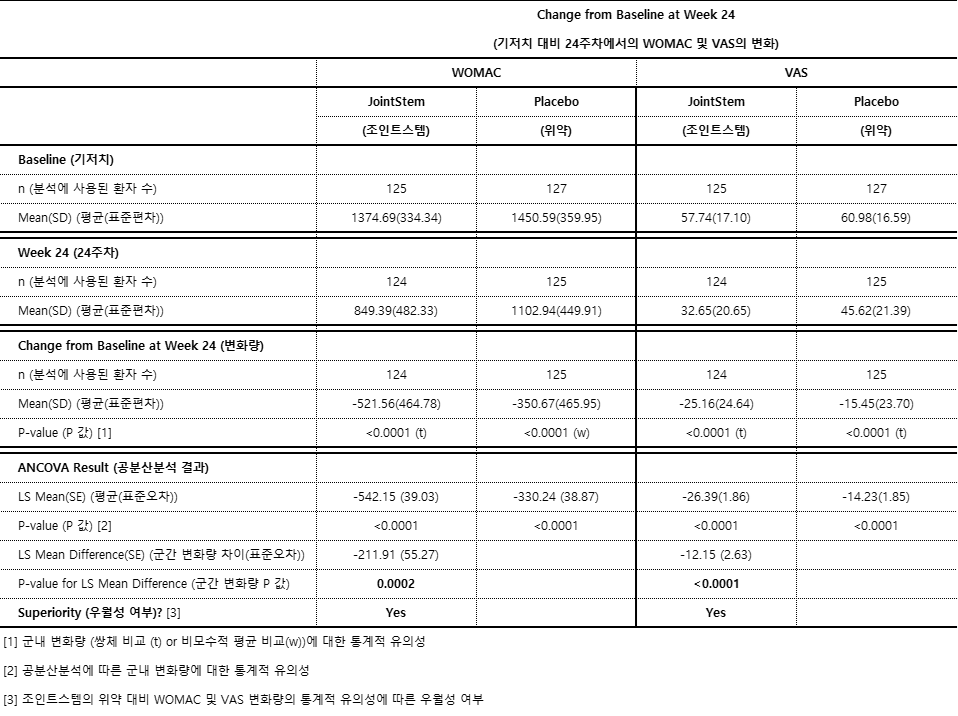
WOMAC의 경우 조인트스템 투여군 환자는 투여 전 평균 1,374.69점에서 투여 24주 후 평균 849.39점으로 521.56점이 감소(P값<0.0001)했으며, 위약 투여군과의 비교에서도 치료 효과가 통계적으로 유의미하게 개선(P값=0.0002)된 것으로 평가됐다.
VAS 또한 조인트스템 투여군 환자는 투여 전 평균 57.74점에서 투여 24주 후 평균 32.65점으로 25.16 점이 감소(P값<0.0001)했고, 위약 투여군과의 비교에서도 통계적으로 유의하게 통증이 감소(P값<0.0001)했음을 확인했다.
일반적인 통계 분석에서 결과치가 0.05 이하이면 성공, 0.05를 초과하면 통계적 유의성 확보에 실패한 것으로 평가하는 지표인 P값도 기준값 대비 크게 낮은 수치를 보였다.(도표 참조)
알바이오가 개발하고 네이처셀이 국내 판매권을 보유하고 있는 조인트스템은 K-L 3등급 이상의 중증 퇴행성관절염 환자를 단 한번의 주사로 치료하는 줄기세포치료제로, 2008년 5월 식약처로부터 국내 임상 1/2상을, 2014년 임상 2b상을 승인받은데 이어 2019년 1월 임상 3상 승인을 받았다.
또, 이와는 별도로 미국에서 임상 2상을 완료한데 이어 최근에는 FDA로부터 2b/3a상 임상계획 승인을 받았다.
서울대병원, 세브란스병원, 강동경희대병원 등 전국 13개 대학병원에서 실시한 임상 3상에는 모두 261명의 중증 퇴행성관절염 환자가 등록, 이 가운데 중도 탈락 및 동의 철회한 환자를 제외한 최종 252명에게 무작위 배정을 통하여 이중맹검을 유지한 채 조인트스템 또는 위약을 투여했다. 이후 6개월 동안의 추적관절을 통해 WOMAC과 VAS를 포함, 유효성 및 안전성에 대한 다양한 평가를 받는 방식으로 진행됐다.
조인트스템 연구 개발 총책임자인 바이오스타 줄기세포기술연구원의 라정찬 박사는 “많은 어려움 속에서도 연구 개발에 함께 하는 분들께 감사하다. 5월까지 최종 결과 보고서를 받고 신약허가 신청을 잘 준비하겠다.”고 의견을 피력했다.